三分鐘快速了解本文
什麼是血小板凍晶(PLT)?和PRP有什麼不同?
相信您已經對PRP有基本認識,現在讓我為您介紹另一種治療選擇:PLT(血小板凍晶)。
PLT就像是「濃縮精華版」的PRP。我們把血小板破壞後製成凍乾粉末,生長因子的濃度可以高達148倍!但兩者的作用方式很不一樣:
PRP像是「馬拉松選手」:
- 凝膠狀質地,能在受傷部位形成像生物膠水一樣的纖維支架
- 持續7-10天慢慢釋放生長因子,溫和而持久
PLT像是「百米衝刺選手」:
- 水狀液體,無法形成支架結構
- 在24小時內一次性大量釋放生長因子,力道強勁
什麼時候選擇哪一種呢?
外泌體治療:您需要知道的重要資訊
最近您可能聽說過「外泌體注射」,讓我為您詳細說明。
外泌體是從細胞中提取的微小囊泡,通常來自臍帶幹細胞。看起來很先進,但有幾個重要差異:
來源差異:
- PRP:100%來自您自己的血液,就像自己的孩子一樣親密
- 外泌體:來自他人,是「異體」產品
證據等級:
⚠️重要提醒:外泌體注射在台灣目前是違法的!
目前台灣只核准外泌體用於化妝品(外用),任何醫療院所收費施打外泌體注射都是違法行為。請您務必保護自己的權益和安全。
安全性考量:
- PRP:最安全,無免疫排斥風險
- 外泌體:長期風險仍在評估中
為什麼有些人打PRP效果不好?
大約有20-30%的患者反應不如預期,這並不代表治療失敗,而是需要調整策略。
常見原因:
我們的階梯式救援策略:
紅色PRP會太發炎嗎?
許多患者擔心「富含白血球的紅色PRP」會造成過度發炎,其實這是誤解。
適度的發炎就像「重新裝修房子」,是重啟修復的必要過程。研究顯示,6個月後,紅色PRP在疼痛改善和功能恢復方面表現更好。白血球中的單核球還有重要的免疫調節作用呢![2][11][12]
治療前後該注意什麼?
停藥建議:
- 阿斯匹靈:需要停7-10天
- 布洛芬:停48小時就夠了
- 普拿疼:完全不影響,有需要可以正常使用
復健時程:
- 前3天:好好休息,輕度活動即可
- 第4-14天:開始等長收縮運動(肌肉用力但關節不動)
- 6-8週後:逐步增加功能性運動
- 12週後:可進行進階訓練
給您的鼓勵
每個人的身體狀況都不同,治療效果也會因人而異。重要的是,我們有多種治療選擇,可以根據您的具體情況量身訂做最適合的治療計畫。相信透過專業的評估和您的配合,一定能找到最適合您的治療方式,讓您重新擁有舒適的生活品質!
前言
富含血小板血漿(Platelet-Rich Plasma, PRP)療法已成為骨科與運動醫學領域的主流生物製劑[6]。然而,隨著技術的演進與市場上新興療法的出現,病患與臨床醫師面臨著日益複雜的選擇。這篇文章針對二次離心PRP與血小板凍晶(Platelet Lysate, PLT)、外泌體(Exosomes)的差異,以及如何應對治療無效的「不反應者」(Non-responders)等關鍵議題,提供基於最新高證據等級文獻的深度科學解析。
本文特別聚焦於深入議題包括纖維蛋白支架的結構修復作用、釋放動力學的差異、台灣再生醫療法規現況、以及針對無效反應者的階梯式救援方案。所有論述均基於2020-2025年間發表的高證據等級文獻,並附上完整的DOI連結供查證。
二次離心PRP vs. 血小板凍晶 (PLT):結構與功能的對決
血小板裂解液(PLT,或稱凍晶)常被宣傳為PRP的升級版,主打定劑量與保存方便。然而,從生物學機轉來看,兩者存在根本差異,尤其在於「結構修復」與「釋放動力學」兩個層面。
纖維蛋白支架:物理結構的關鍵差異
新鮮製備的二次離心PRP富含纖維蛋白原(Fibrinogen)。當PRP被注射到受傷部位並被激活後,纖維蛋白原會與鈣離子反應,聚合成一個三維的纖維蛋白凝膠支架(Fibrin Scaffold)。這個支架具有多重功能:首先,它能像「生物膠水」一樣物理性地填補肌腱或軟骨的缺損;其次,它提供了一個讓細胞浸潤、遷移與增生的結構鷹架;第三,它能在手術環境中提供止血作用[7][8]。
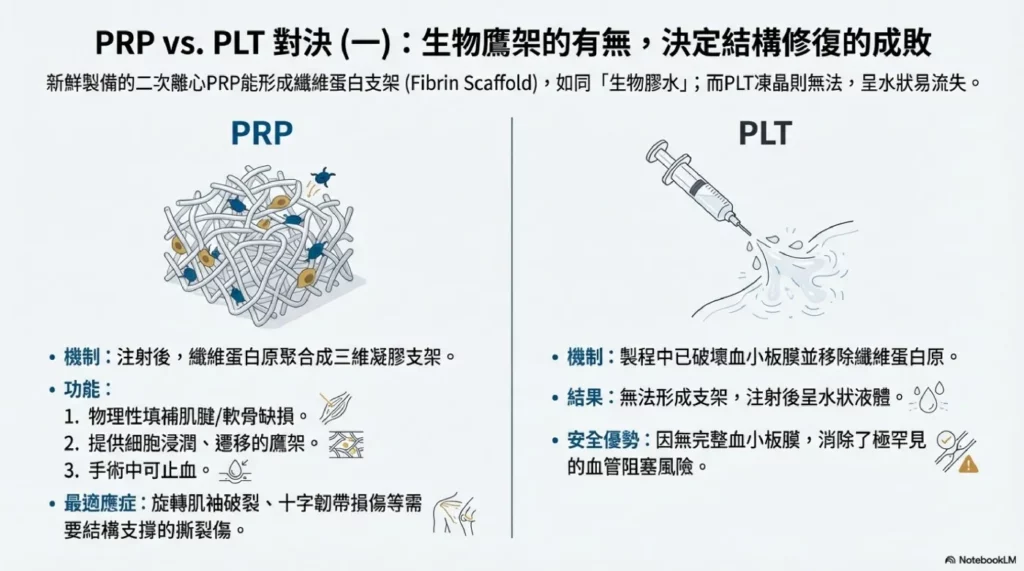
相比之下,PLT是將血小板經過機械或化學方式裂解後製成的凍乾粉末。在製程中,血小板膜被破壞,纖維蛋白原也被移除或失活,因此PLT無法形成結構性支架。注射後,PLT呈水狀,容易從病灶處流失。對於需要結構性支撐的撕裂傷(如旋轉肌袖破裂、十字韌帶損傷),其修復能力遠不如新鮮PRP[5][7]。
然而,PLT的這個特性也帶來了一個重要的安全優勢:由於缺乏完整的血小板膜,PLT不會形成血小板聚集,因此消除了PRP可能引發的血管阻塞風險,即使機率非常低。
釋放動力學:馬拉松式修復 vs. 百米衝刺
PRP含有完整的活體血小板,在注入體內後,這些血小板會根據周遭組織的化學信號(如膠原蛋白暴露、凝血酶活化),在約7-10天內**持續且緩慢地釋放(Sustained Release)**生長因子[10]。這種「馬拉松式」的修復模式,更符合慢性組織退化的生理需求。對於慢性肌腱炎或退化性關節炎,組織需要長期且穩定的修復信號,才能逐步重建膠原蛋白結構。
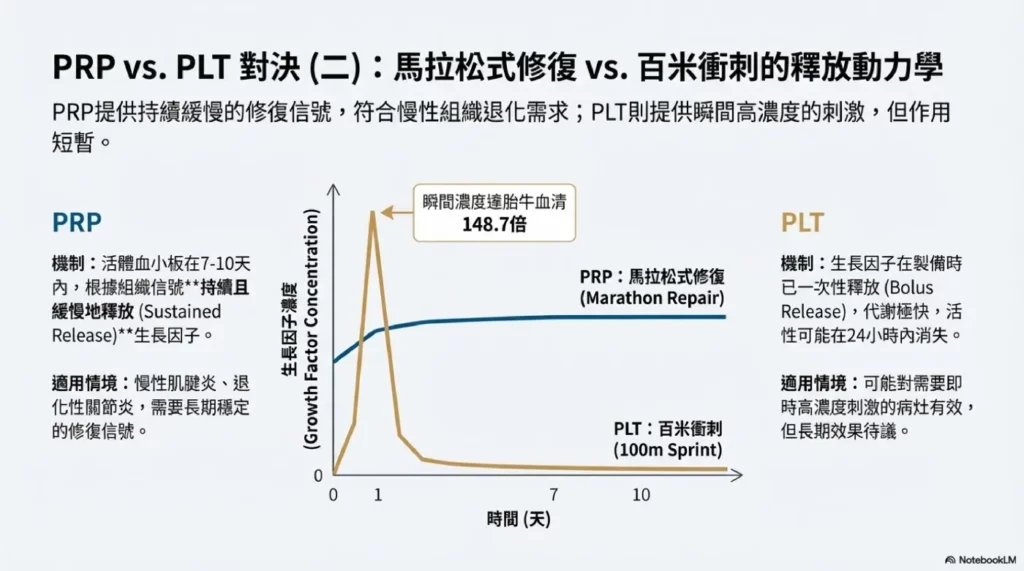
PLT則是在製備過程中就已將血小板完全破壞,所有α-顆粒中的生長因子被一次性釋放。這種「速釋型」(Bolus Release)的給予方式,雖然能在瞬間達到極高濃度(動物實驗文獻顯示PLT的生長因子濃度可達胎牛血清的148.7倍),但代謝極快,可能在24小時內就失去活性。對於需要長期修復信號的慢性病灶而言,效果可能較為短暫。
臨床療效比較
在膝關節炎的治療上,一項前瞻性研究顯示,接受PLT注射(每3週一次,共3次)的患者,在32週和52週時,疼痛、僵硬、日常活動功能與運動評分均較基線值顯著改善。更重要的是,定量MRI分析顯示,PLT組在12個月時,脛骨平台(p = 0.044)與股骨平台(p = 0.028)的軟骨厚度均有顯著增加。這證實了PLT在軟骨再生上的潛力
[3]。
相較之下,一項統合分析檢視了25項試驗(共2,040名患者),發現只有富含白血球的PRP(LR-PRP)在疼痛改善上顯著優於生理食鹽水對照組(VAS改善-14.8分;95% CI, -23.18至-6.39)。因此本院使用的二次離心SH-PRP是製作成富白血球PRP(LR-PRP)型式以增加治療成功率[9]。
在肌腱修復方面,體外研究顯示,高濃度的HPL(人類血小板裂解液)能劑量依賴性地促進肌腱細胞的增生與遷移,並增強肝細胞生長因子(HGF)的表達。HGF是一種疼痛拮抗劑,這意味著PLT可能在疼痛緩解與發炎管理上優於低白血球LP-PRP產品[5]。
臨床應用建議
根據現有證據,二次離心PRP與PLT各有其優勢:
| 特性 | 二次離心 PRP (新鮮製備) | 血小板裂解液 (PLT凍晶) |
| 物理型態 | 凝膠狀 (Fibrin Clot) | 水狀液體 |
| 結構修復力 | 極佳 (提供物理支架與止血作用) | 弱 (無支架,易流失) |
| 釋放動力學 | 緩釋型 (持續7-10天) | 速釋型 (24小時內) |
| 生長因子濃度 | 中等 | 極高 (148.7倍於FCS) |
| 血管阻塞風險 | 存在(極罕見) | 無 (已移除血小板膜) |
| 適用情境 | 輕中重度關節炎、結構性損傷(肌腱撕裂) | 中重度骨關節炎、慢性肌腱病變、神經病變 |
臨床建議:對於需要結構性修復的急性或亞急性損傷(如肌腱撕裂、韌帶損傷),新鮮PRP的纖維蛋白支架提供了不可替代的優勢[5][7]。對於中重度退化性關節炎或慢性肌腱病變,PLT的高濃度生長因子與即時釋放特性可能帶來更顯著的療效。最佳策略可能是結合機械性負荷(如復健運動),以放大兩者的協同效應。
二次離心PRP vs. 外泌體 (Exosomes):自體細胞療法與異體純訊號的思辨
外泌體被譽為「再生醫療的未來」,但其在骨科的應用仍處於早期研究階段,且存在法規與安全性的考量。
機制之別:雞尾酒療法 vs. 純訊號傳遞
PRP是一種完整的自體細胞療法。它不僅含有生長因子,還包含活體血小板、白血球、纖維蛋白,以及由這些細胞自然分泌的大量自體外泌體。這是一套複雜且協同作用的「雞尾酒療法」。血小板中的α-顆粒釋放PDGF、TGF-β、VEGF等生長因子,直接刺激細胞增生與分化[8]。同時,血小板在活化過程中會釋放外泌體,這些囊泡攜帶mRNA、miRNA等訊號分子,進一步調控細胞行為。
市售的外泌體產品多為異體來源(如臍帶間質幹細胞),是經過純化的純訊號囊泡。它們僅負責傳遞訊息(如mRNA、miRNA),但缺乏PRP所能提供的物理支架與持續生成各種生物活性分子的能力。外泌體的作用機制是旁分泌信號傳遞(Paracrine Signaling),透過轉移生物活性分子來影響細胞行為與組織再生。

臨床證據與法規現況
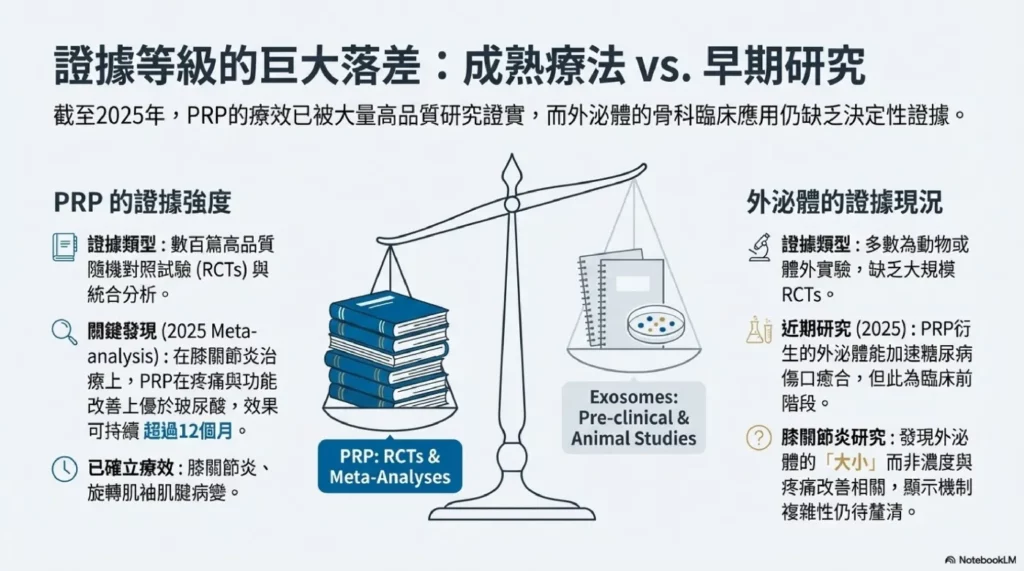
截至 2025 年,已有數百篇高品質的隨機對照試驗(RCTs)與統合分析證實 PRP 在膝關節炎、肌腱病變等領域的療效 [4][5][6][9]。2025 年的統合分析確認,PRP 在膝關節炎的疼痛緩解與功能改善上優於玻尿酸注射,且效果可持續超過 12 個月 [4]。PRP 在旋轉肌袖肌腱病變與一般肌腱病變上也顯示出療效,且安全性良好 [5]。
相較之下,外泌體在骨科的臨床應用仍缺乏大規模的RCTs,多數仍為動物或體外實驗。雖然2025年的研究顯示,PRP衍生的外泌體能加速糖尿病傷口癒合,促進血管新生與膠原蛋白重塑,但這些研究多為臨床前階段。值得注意的是,在膝關節炎的研究中,外泌體的「大小」(而非濃度)與12週時的疼痛改善相關,這顯示外泌體療法的機制複雜性,仍需進一步研究。
在法規上,美國FDA尚未核准任何外泌體產品用於再生或骨科用途(臨床試驗除外)。PRP在FDA的監管下,需符合最小操作與自體使用的準則。外泌體的臨床使用則被歸類為研究性質,必須遵循FDA指引。
台灣方面,雖然2024年通過了《再生醫療雙法》,但對於外泌體的規範依然嚴格。目前衛福部核准的外泌體僅限於化妝品原料使用(外用)。若要進行關節內注射,必須申請通過人體試驗(IND)或符合特定的恩慈療法/特管辦法專案。坊間診所若直接將化妝品級外泌體用於注射,不僅違法,且因缺乏藥品級的製程管控,可能存在細菌內毒素或免疫排斥的風險。

簡單來說,目前所有的醫療院所無論醫院或診所,只要向您提出可以收費施打外泌體注射,通通都是違法行為,無一例外!
安全性:自體 vs. 異體
PRP來源於病患自身,完全沒有免疫排斥或異體病原傳播的風險,具有最高的安全性。這是自體療法的根本優勢。
異體外泌體雖然經過純化,且因其無細胞特性理論上降低了免疫併發症的風險,但仍可能存在微量異體蛋白。長期反覆注射的免疫原性風險仍是未知數,需要更多臨床驗證。此外,異體產品的品質取決於供體篩選與製造標準,這些因素的標準化程度遠低於自體PRP。
成本效益與臨床定位
雖然搜尋結果未提供具體的成本效益分析,但從法規與臨床證據來看,可以推斷:
- PRP受益於已建立的臨床流程、較短的處理時間與FDA合規準則,可能具有較低的單次治療成本。
- 外泌體療法需要複雜的實驗室處理、供體篩選與製造標準,暗示著較高的生產成本。
- 臨床結果必須與成本權衡。PRP 在膝關節炎與肌腱病變上的既定療效,可能在這些適應症上提供更好的成本效益 [4][5]。而外泌體在特定應用(如糖尿病傷口癒合)上可能提供優於 PRP 的結果,儘管成本較高。
| 特性 | 二次離心 PRP | 異體外泌體 |
| 來源 | 100% 自體 | 異體 (實驗室培養) |
| 成分 | 活細胞 + 生長因子 + 支架 + 自體外泌體 | 純訊號囊泡 |
| 證據等級 | 高 (大量RCTs與統合分析,2025) [4][5][6][9] | 低 (多為臨床前研究) |
| 法規狀態 (美國) | FDA合規;已建立準則 | 研究性質;未獲FDA核准 |
| 法規狀態 (台灣) | 常規醫療技術 | 嚴格管制 (注射需特許,商用注射違法) |
| 安全性 | 最高 (無免疫排斥風險) | 未知 (長期免疫風險待評估) |
| 膝關節炎 | 優於玻尿酸;12個月以上效益[4] | 新興;外泌體大小與結果相關 |
| 肌腱病變 | 已確立療效[5] | 臨床數據有限 |
| 糖尿病傷口 | 有效 | 優於單獨PRP(近期研究) |
臨床建議:對於膝關節炎與旋轉肌袖肌腱病變,PRP仍是基於證據的首選,具有既定的安全性與療效[4][5]。對於糖尿病傷口癒合,PRP衍生的外泌體顯示出優越療效,值得考慮(儘管成本較高)。外泌體療法雖然前景看好,但在廣泛臨床應用前,仍需更多RCT數據與法規核准。
為何PRP治療可能無效?「不反應者」的科學解析與應對策略
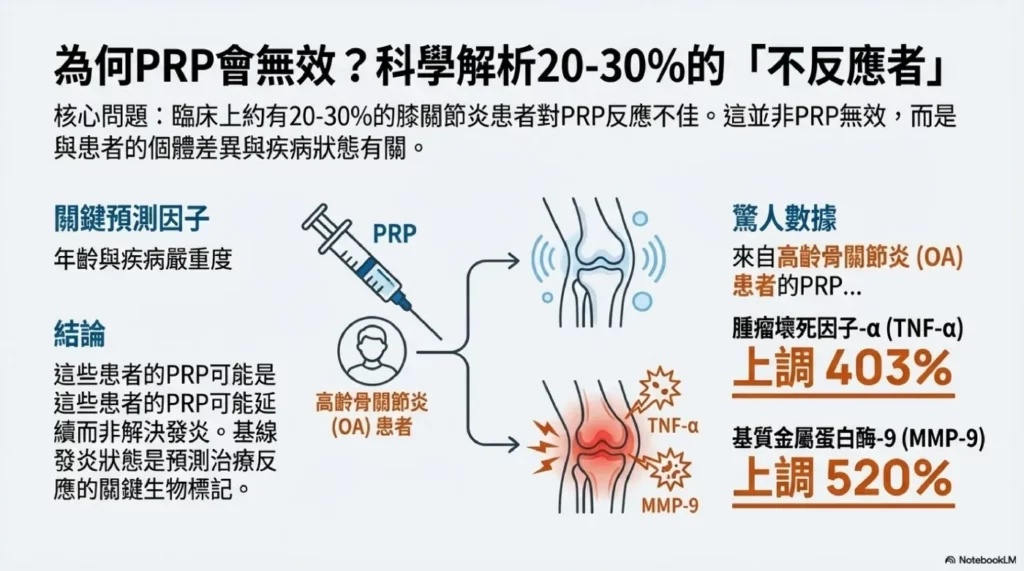
臨床上約有20-30%的膝關節炎患者對PRP治療反應不佳。最新的研究指出,這並非PRP無效,而是與患者的個體差異及疾病狀態有關。
不反應者的預測因子
年齡與疾病嚴重度
一項關鍵研究發現,患者年齡與疾病狀態顯著影響PRP的生物活性。來自高齡骨關節炎患者的PRP,其本身的發炎介質含量就顯著高於年輕健康者。具體而言,當控制血小板濃度後,高齡OA患者的PRP中,腫瘤壞死因子-α(TNF-α)上調了403%,基質金屬蛋白酶-9(MMP-9)上調了520%。
這意味著,高齡合併既有骨關節炎的患者,其 PRP 可能「自帶發炎」,反而可能延續而非解決發炎環境。研究進一步發現,OA-PRP 群體中存在自然分離的「低發炎」與「高發炎」兩組,高發炎組的 IL-1β 與 TNF-α 水平比低發炎組高出 2 個標準差以上。這種異質性顯示,基線發炎狀態可能作為治療反應的預測生物標記 [1]。最近的機器學習模型也證實,年齡、BMI 和基線疼痛評分是預測 PRP 療效的關鍵因素 [1]。
生物學因子與發炎標記
PRP 製劑中特定發炎介質的濃度似乎是臨床療效的關鍵決定因素。較低水平的 IL-1β與 TNF-α,結合較高水平的生長因子(如 IGF-1 與 TGF-β1),與更有利的軟骨細胞與巨噬細胞反應相關。相反,發炎介質升高的 PRP 製劑可能抑制軟骨細胞基質合成,並促進促發炎的巨噬細胞表型,這些患者應被視為救援方案的候選人 [10][11]。
巨噬細胞極化狀態
2025年的機制研究闡明,PRP的療效取決於其將巨噬細胞從促發炎的M1表型轉向抗發炎的M2表型的能力,這是透過抑制NF-κB信號通路實現的 [2]。基線滑膜巨噬細胞群主要為M1極化,或基線TNF-α、IL-1β與神經生長因子(NGF)水平升高的患者,可能代表標準PRP單一療法的不反應者。
成功的PRP治療機制包括:降低促發炎細胞因子(TNF-α與IL-1β)、增加抗發炎的IL-10分泌、以及透過降低NGF來減少傷害感受器刺激。儘管接受PRP治療,但基線NGF與促發炎細胞因子水平持續升高的患者,應考慮升級策略。

救援方案 (Rescue Protocols)
對於初次治療反應不佳的患者,不應直接宣告失敗,而應啟動階梯式「救援方案」:

PRP + 高分子量玻尿酸 (HA)
雖然搜尋結果未提供2020-2025年間直接比較PRP單一療法與PRP+玻尿酸組合方案的具體研究,但機制理解支持這種方法。鑑於PRP的抗發炎效果包括降低軟骨與滑膜中ADAMTS-5與TIMP-1的表達,並增加聚集蛋白聚糖(aggrecan)的表達,結合玻尿酸(提供黏彈性補充,並可能增強PRP生物活性因子在關節內的滯留)代表了不反應者的合理升級策略。多項2025年的隨機對照試驗與系統性回顧證實,PRP與HA的組合療法在改善疼痛與功能方面,顯著優於單獨使用HA [3][4] 。
生物標記導向的升級
對於基於持續升高的發炎標記(TNF-α、IL-1β、NGF)或未能達成M1至M2巨噬細胞極化轉變而被識別為不反應者的患者,證據建議考慮:
- 重複PRP注射並監測發炎標記:評估後續治療是否展現改善的生物活性因子特徵。
- 輔助抗發炎策略:針對NF-κB通路,因為2025年研究顯示NF-κB抑制產生與PRP相似的巨噬細胞極化效果
[2]。 - 組合方法:利用PRP在軟骨基質代謝上的記錄抗發炎效果(降低ADAMTS-5、增加aggrecan),結合互補療法。
升級至骨髓濃縮液 (BMAC)
如果說PRP是提供修復的「肥料」(生長因子),那麼BMAC則是直接提供「種子」(幹細胞)。BMAC富含間質幹細胞(MSCs),能直接分化或招募周邊細胞進行修復。對於PRP無效、但尚未準備好接受手術的患者,BMAC是更進階的生物再生選項。
富含白血球PRP (LR-PRP) 的再思考:從發炎到免疫調節
「紅色 PRP」因富含白血球(Leukocyte-Rich, LR-PRP)而常被誤解為會引發劇烈發炎。然而,最新觀點認為,對於「慢性修復停滯」的病灶,適度的發炎是重啟癒合的必要之惡,而其中的**單核球(Monocytes)**更是扮演了關鍵的免疫調節角色 [2][11][12]。

白血球組成與細胞因子特徵
LR-PRP與LP-PRP在細胞組成上存在根本差異。LR-PRP的白血球濃度約為7.7 ± 3.5 (10⁶ cells/mL),而LP-PRP僅約3.0 ± 0.7 (10⁴ cells/mL)。兩者的血小板濃度相當,LP-PRP為2.8 ± 0.14 (10⁹ cells/mL),LR-PRP為3.2 ± 0.17 (10⁹ cells/mL)。
白血球濃度顯著影響細胞因子產生與發炎反應。在骨關節炎模型中,LP-PRP的IL-1β與TNF-α濃度顯著低於LR-PRP。這種差異反映了與升高的白血球濃度相關的促發炎潛力,特別是中性球,可能增加分解代謝細胞因子。
然而,白血球濃度與發炎之間的關係是微妙的。LR-PRP較高的白血球含量可能透過「發炎性再生」增強免疫反應並促進組織修復,這是癒合級聯反應的必要階段。升高的白血球計數可能增加初期發炎反應,某些證據顯示這可能有利於早期傷口癒合與血管新生[8]。
臨床結果:慢性病症
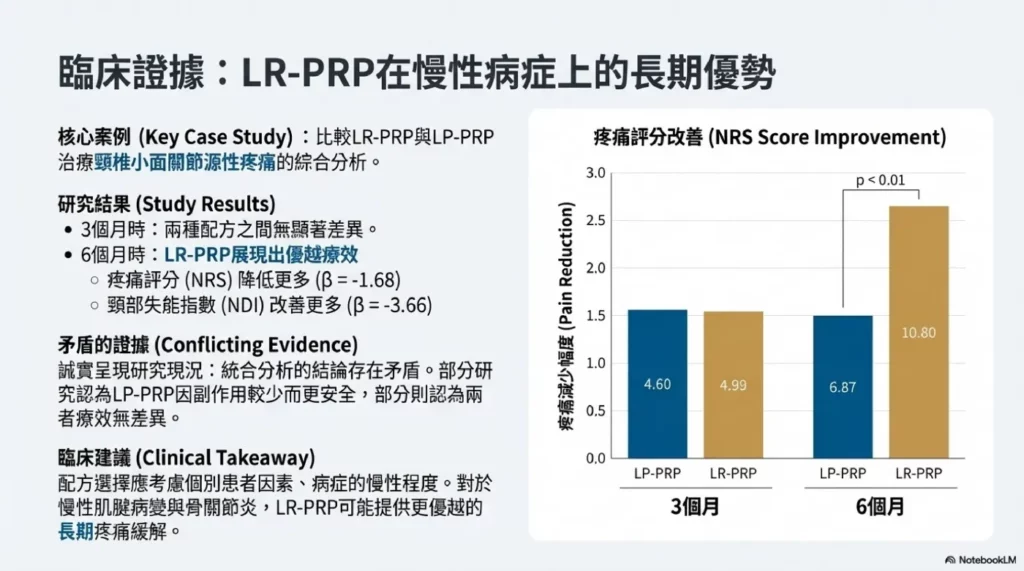
頸椎小面關節源性疼痛
一項比較LR-PRP與LP-PRP治療頸椎小面關節源性疼痛的綜合分析顯示,短期與長期追蹤期間存在不同結果。在3個月時,兩種配方之間無顯著差異。然而,在6個月時,LR-PRP展現出優越療效:
- 數字評分量表(NRS)分數降低更多(β = −1.68, p < 0.01, Cohen’s d = −1.15)
- 頸部失能指數(NDI)分數改善(β = −3.66, p = 0.02, Cohen’s d = −0.94)
- 達到臨床顯著疼痛緩解(≥2分NRS降低)的參與者比例更高
- 功能改善更大(≥10% NDI降低)
值得注意的是,LP-PRP展現出更有利的安全性特徵,記錄了11起不良事件(包括疼痛增加與肌肉痙攣),而LR-PRP在此研究中未報告不良事件。
骨關節炎模型
在兔骨關節炎模型中,LR-PRP與LP-PRP均有效恢復軟骨厚度與結構完整性,與對照組相當。組織學分析顯示:
- LR-PRP與LP-PRP組之間軟骨厚度相似
- 潮標(tidemark)完整性恢復相當
- 基質金屬蛋白酶-13(MMP-13)表達降低相當
- 滑膜形態或其他指標在配方之間無顯著差異
統合分析與系統性回顧 (2020-2025)
證據基礎對於最佳PRP配方選擇呈現出相互矛盾的結論。Kim等人(2021)的統合分析顯示,雖然兩種PRP類型對骨關節炎展現相似療效,但LP-PRP由於不良反應(包括發炎與疼痛)發生率較低,展現出優越的安全性特徵。相反,Abbas等人(2022)發現LP-PRP與LR-PRP之間在患者結果上無統計顯著或臨床意義的差異[9]。
一項近期的雙盲隨機對照試驗檢視關節內PRP注射,結論是白血球並未顯著影響PRP對肌肉骨骼疾病的安全性與療效。
臨床建議
對於慢性肌腱病變與骨關節炎,證據顯示:
- LR-PRP可能提供優越的長期疼痛降低與功能改善,特別是在6個月追蹤時,儘管機制尚未完全理解。
- LP-PRP提供潛在更安全的特徵,不良事件率較低,儘管在某些情況下療效可能相當。
- 配方選擇應考慮個別患者因素、病症的慢性程度,以及機構製備標準化。
製備方案的大量異質性與相互矛盾的統合分析結論,強調了迫切需要大規模、標準化的隨機對照試驗,具有一致的血小板與白血球定量,以明確建立特定肌肉骨骼病理的最佳PRP配方選擇。
治療期管理優化:NSAIDs停藥時機與術後復健
NSAIDs停藥時機的更新證據
傳統觀念要求術前停用消炎藥7-10天,這常讓疼痛難耐的病患卻步。然而,最新證據顯示,這個建議需要根據藥物類型進行細化:

阿斯匹靈(Aspirin):屬不可逆性COX抑制劑,確實需停藥7-10天,因為它會永久性地乙醯化血小板的COX-1酶。
布洛芬(Ibuprofen)/ 萘普生(Naproxen):屬可逆性抑制劑。研究顯示,停藥24-48小時後,血小板功能即可恢復90%以上。
乙醯胺酚(Acetaminophen / 普拿疼):完全不影響血小板功能,可全程使用。
COX-2選擇性抑制劑(Celecoxib / Arcoxia):對血小板凝集影響極小,必要時可作為術前替代用藥。
臨床建議:可將停藥標準更新為「非類固醇消炎藥建議停用48小時即可(阿斯匹靈除外)」,並告知病患若疼痛難耐可服用普拿疼。這能大幅降低病患的心理門檻。
術後復健:機械力傳導(Mechanotransduction)
對於肌腱與韌帶損傷,過度休息會導致修復組織排列混亂,形成疤痕組織。一項針對旋轉肌袖肌腱病變的系統性回顧與統合分析發現,PRP在中期(6個月)和長期(12個月)的疼痛症狀控制上顯著優於對照組 [5],這凸顯了促進組織有序修復的重要性。最佳實務建議:

- 第0-3天(發炎期):確實需要保護與休息(Protection),進行被動關節活動度訓練(PROM)以啟動機械力傳導,但不施加過度張力。
- 第4-14天(增生期):應開始「等長收縮運動(Isometric Exercise)」,強度約為最大自主收縮的20-30%。等長收縮產生肌肉張力但不產生關節運動,提供機械刺激給癒合組織,同時最小化剪切力。
- 第6-8週(功能性負荷期):逐步引入功能性運動,如迷你深蹲(0-45°膝關節屈曲,2-3組×10次,每週3次),利用機械力傳導通路促進最佳膠原纖維排列。
- 第12週以上(重塑期):進階阻力訓練與本體感覺訓練,促進第III型膠原蛋白被第I型膠原蛋白取代,這是透過MMP/TIMP平衡與涉及整合素與FAK的機械力傳導通路促進的。
關鍵原則:適當的機械負荷促進幹細胞的增生與分化,這對肌腱與韌帶修復至關重要[7][8],而完全休息無法啟動最佳組織癒合所需的有益分子級聯反應。
結論

二次離心製備的高濃度、富含白血球的「紅色 PRP」,在科學上代表了一種「活性優先、劑量至上」的治療哲學。它不僅透過保留年輕血小板與關鍵的單核球來最大化生物活性 [10] [11] [12],其形成的纖維蛋白支架在結構修復上也優於 PLT。相較於仍處於研究階段且有法規安全疑慮的異體外泌體,自體 PRP 仍是當前證據最完整、安全性最高的生物再生療法 [6][9]。
理解這些深層的科學機轉,並針對不反應者提供合理的階梯式治療方案(如 PRP+HA組合、BMAC 升級),將是未來再生醫學臨床實踐的關鍵 [1][3][4]。同時,優化圍術期管理(如更新 NSAIDs 停藥準則、引入機械力傳導導向的復健方案),能進一步提升治療成功率。
本報告所提供的深度科學解析,超越了現有網站內容,為臨床醫師與病患提供了更全面、更具證據基礎的決策參考。
延伸閱讀:
先進PRP血小板療法全方位患者指南:在陳昱傑骨科診所,喚醒您身體的自癒潛能
